
细菌与人类健康息息相关,它既是塑造高等生命的天使,也是带来人间疾苦的魔鬼,每年常规造成数亿人患病、近千万人死亡。抗生素的发现,近百年来挽救了无数生命,但目前面临着诸多困境。细菌持留(Persistence)是困境之一,导致临床抗感染治疗长周期、病情反复、耐药突变等风险频发。持留自1942年首次报道以来,其分子机理仍未完全阐明,目前临床尚缺乏能高效杀灭常见病原细菌持留菌的抗生素。
持留一般指细菌群体经抗生素充分杀伤后、依然有部分细胞(持留菌)存活的现象,表现为亚群行为,其特征是敏感菌被快速杀灭、持留菌的存活曲线下降极其平缓(图1)。持留不改变药物最小抑菌浓度,持留水平因不同菌而异。由于经典抗生素致死效应往往依赖胞内活性氧自由基(ROS;该发现直到近十几年才被提出与验证),外加生命系统和实验条件的复杂性,使得持留与耐受(Tolerance;通常是群体行为)的存活表型在实际实验观测中经常难以区分。
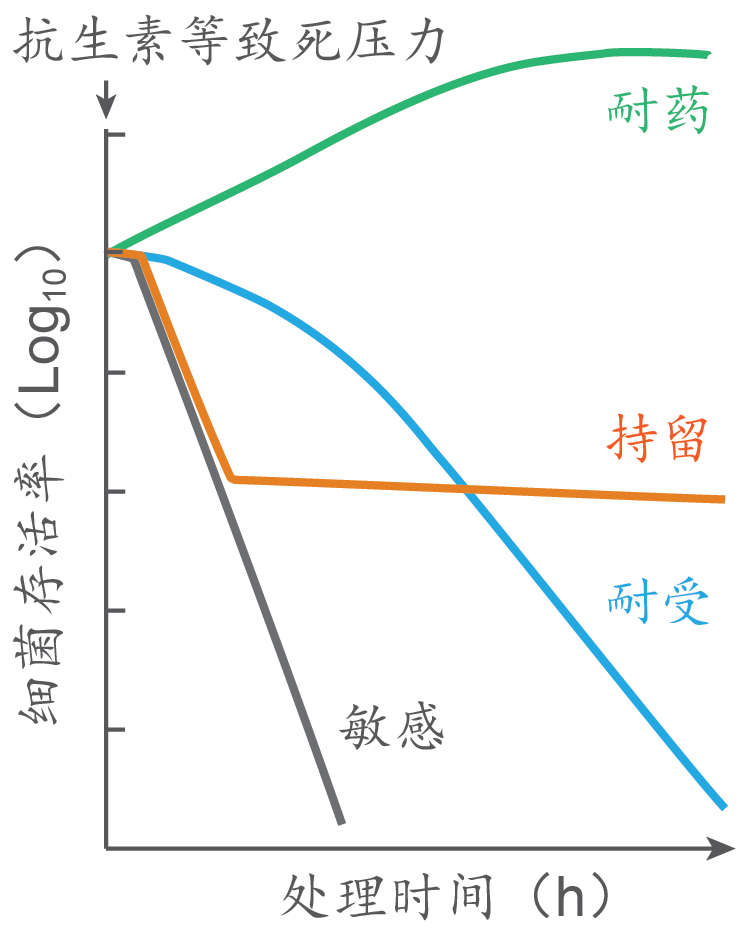
图1 持留、耐受、耐药的示意图
近期,苏州大学洪宇植教授团队在mBio发表文章,揭示持留因内源静息(Endogenous quiescence)导致,不同持留水平(0.001%−10%)大肠杆菌培养物中的细胞一旦进入持留态,在外源营养物和五大类杀伤型抗生素的合力夹击下,依然“百毒不侵、傲然于世”(图2)。(注:五大类抗生素为内酰胺、氨基糖苷、喹诺酮、多粘菌素、丝裂霉素。此谓:细胞持留凭静息,梦里御敌万千兵。)

与内源静息性持留菌不同,外源营养物部分饥饿(如平台期)或完全营养饥饿(生理盐水孵育)的野生型大肠杆菌培养物,几乎完全存活于上述抗生素,然而杀伤过程中只要添加新鲜营养,则导致快速死亡5个数量级。因此,外源营养丰度等环境因素限制了抗生素的致死效应,导致群体细胞存活(称为表观耐受,Phenotypic tolerance),其胞内实则已经做好响应抗生素而死亡的物质准备,因而在机理上与持留有本质差异(图2、图4)。(注:表兄耐受机理异,药食同炉现原形。)
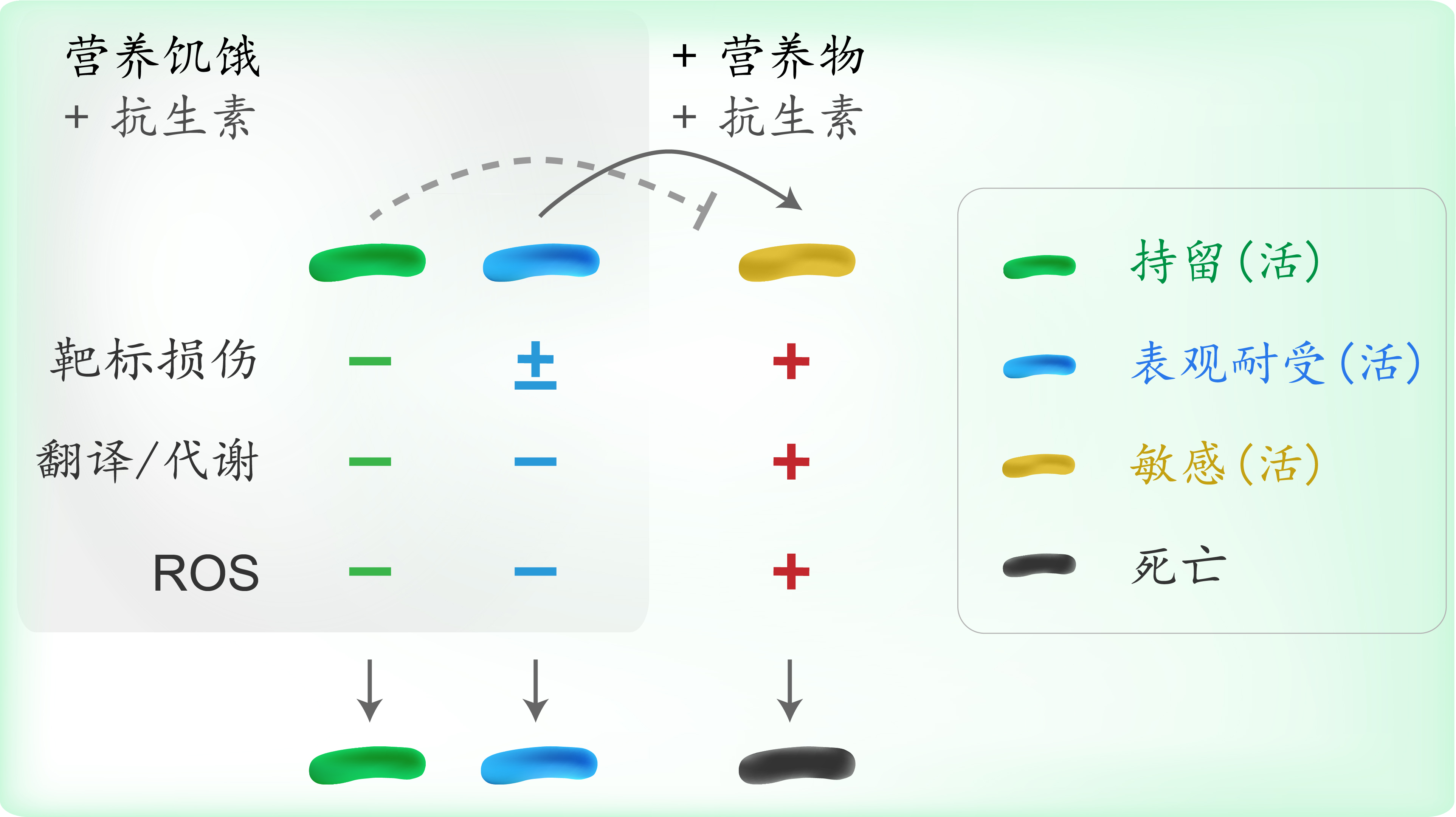
图2 持留与表观耐受的异同
持留菌的内源静息机 制,造成“三少”:抗生素靶标损伤少、代谢活性少、ROS累积少,现有抗生素在临床血药浓度范围内难以施展用武之地,怎么办?洪宇植团队一直致力于细菌应激死亡和抗生素杀伤机理探索,前期相关成果发表于PNAS(2019、2022、2025,均直投)、Nature Microbiology (2017)等期刊,在这些积累基础上,经广泛筛选小分子化合物库,发现氨基糖苷-多粘菌素联合抗生素(代号“灭绝师太”)通过协同效应获得超强的菌膜穿孔能力,以“ROS不依赖的菌膜直接穿孔”之矢突破持留菌的内源静息“命门”(图3)。(注:破菌灵方何处觅,倚天剑刃在丹青。)
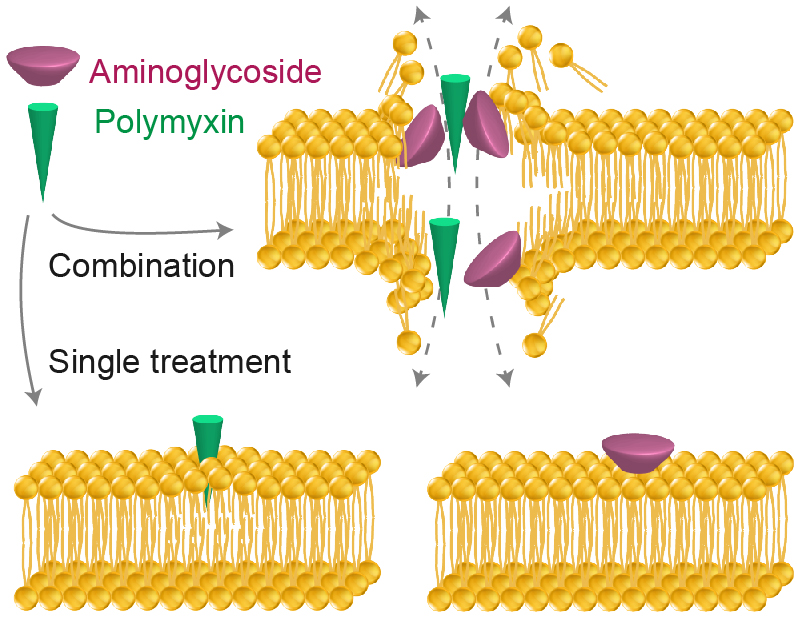
图3 “灭绝师太”破细菌细胞膜的示意图
“灭绝师太”在低于血药峰值的较宽浓度范围内,对大肠杆菌和肺炎克雷伯菌(医院获得性感染排名前二)的持留菌几乎完全清除,对∆cyaA、∆crp、∆ptsI等泛耐受菌株(PNAS2022,119(23): e2118566119)同样几乎完全清除,在数小时内杀灭106−107,对其生物膜菌群杀灭104(而单药在同等浓度下的杀伤效果甚微或完全没有),对金黄色葡萄球菌、绿脓杆菌也有协同杀伤效果,但对人源细胞高度安全。因此,“灭绝师太”首次实现临床血药浓度范围内对常见病原细菌持留菌的大量快速清除,有望成为上述相关细菌临床持留感染病的治疗药物。(注:“灭绝师太”的配方、剂量和效用已授权发明专利,并由一家药企推进临床相关实验。)
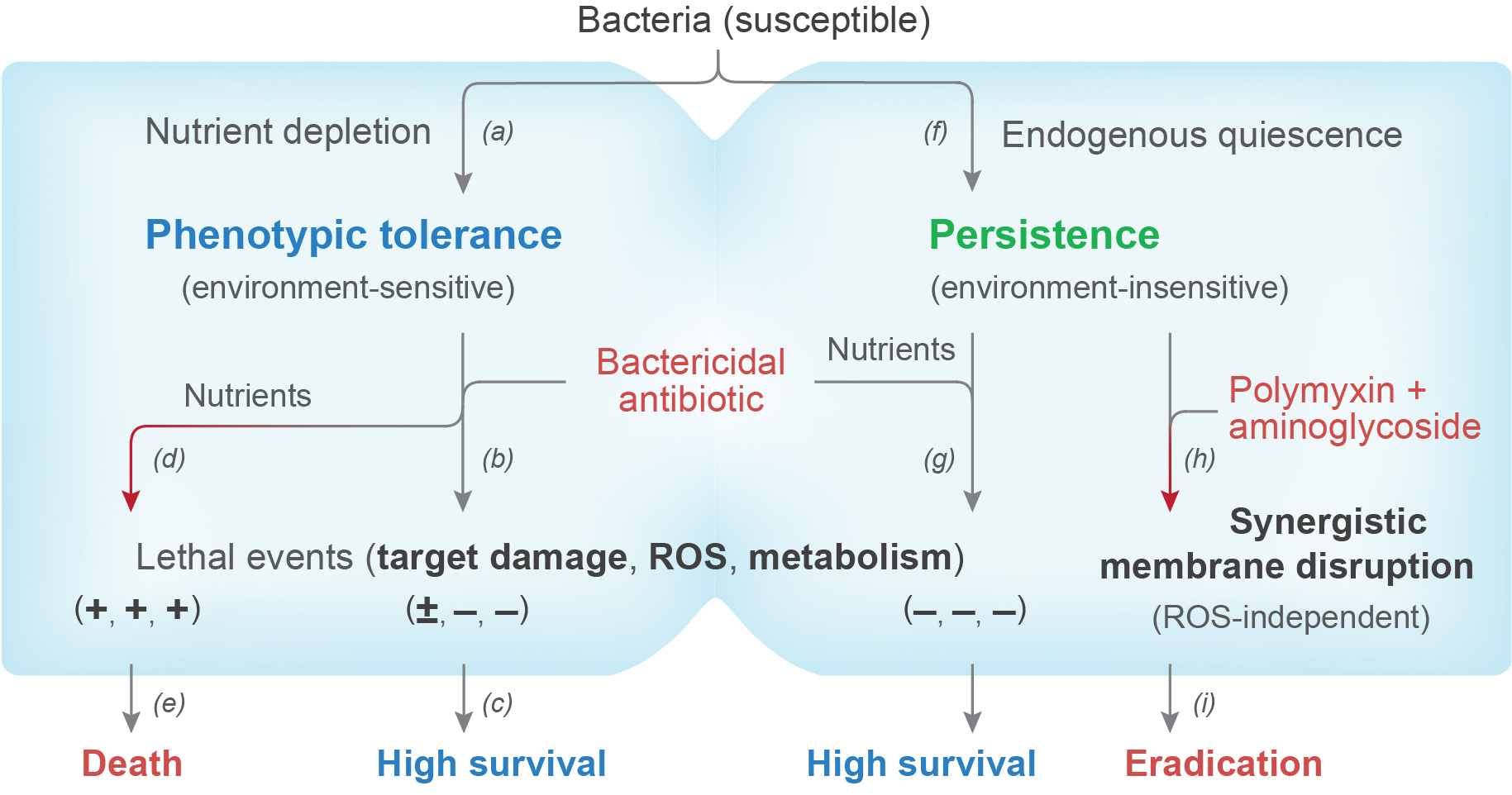
图4 机制概括图
苏州大学苏州医学院生命科学学院、老年病与免疫教育部重点实验室洪宇植教授为论文通讯作者,博士后叶杨慧、博士生田原青、硕士生段明昕为共同第一作者,厦门大学赵西林教授、美国Rutgers大学Karl Drlica教授、苏州大学第一附属医院徐峰主任共同合作研究,博士后朱伟伟、博士生陈意林、硕士生吴静云为共同作者,苏州大学周哲敏、张海方、庄文卓三位教授为研究提供帮助。该工作获国家自然科学基金面上项目、江苏特聘教授项目、苏州市姑苏创新领军项目、中国博士后科学基金、江苏省科教能力提升工程等资助。(论文链接:https://journals.asm.org/doi/10.1128/mbio.01199-25)

